
Теорія вказує, що при одній температурі середні кінетичні енергії молекул m v 2ср / 2 однакові. При нашому визначенні температури ця середня кінетична енергія поступального руху молекул газу пропорційна абсолютній температурі. Комбінуючи рівняння ідеального газу і рівняння Бернуллі, знайдемо
Вимірювання температури термометром, заповненим ідеальним газом, надає цьому заході простий сенс: температура пропорційна середньому значенню енергії поступального руху молекул. Оскільки ми живемо в тривимірному просторі, про точку, що рухається як завгодно, можна сказати: вона має три ступені свободи. Значить, на одну ступінь свободи рухається частинки доводиться кТ / 2 енергії.
Визначимо середню швидкість молекул кисню при кімнатній температурі, яку ми для круглого рахунку приймемо в 27 ° С = 300 К. Маса однієї молекули кисню дорівнює 32 / (6 * 1023). Просте обчислення дасть м ср = 4,8 * 104 см / с, тобто близько 500 м / с. Істотно швидше рухаються молекули водню. Їх маси в 16 раз менше і швидкості в 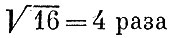 більше, т. е. при кімнатній температурі становлять близько 2 км / с. Парканом, з якою теплової швидкістю рухається маленька? видима в мікроскоп частинка. Звичайний мікроскоп дозволяє побачити порошинку діаметром в 1 мкм (10-4 см). Маса такої частки при щільності ,; близькою до одиниці, буде що-небудь близько 5 * 10-13 м Для її швидкості отримаємо близько 0,5 см / с. Не дивно, що такий рух цілком помітно.
більше, т. е. при кімнатній температурі становлять близько 2 км / с. Парканом, з якою теплової швидкістю рухається маленька? видима в мікроскоп частинка. Звичайний мікроскоп дозволяє побачити порошинку діаметром в 1 мкм (10-4 см). Маса такої частки при щільності ,; близькою до одиниці, буде що-небудь близько 5 * 10-13 м Для її швидкості отримаємо близько 0,5 см / с. Не дивно, що такий рух цілком помітно.
Швидкість броунівського руху горошини з масою в 0,1 г буде вже всього лише 10-6 см / с. Не дивно, що ми не бачимо броунівського руху таких частинок.
Ми говоримо про середніх швидкостях молекули. Але ж не всі молекули рухаються з однаковими швидкостями, якась частка молекул рухається швидше * а якась повільніше. Все це, виявляється можна розрахувати. Наведемо лише результати.
При температурі близько 15 ° С, наприклад, середня швидкість молекул азоту дорівнює 500 м / с, зі швидкостями від 300 до 700 м / с рухається 59% молекул. З малими швидкостями - від 0 до 100 м / с - рухається лише 0,6% молекул. Швидких молекул зі швидкостями понад 1000 м / с в газі лише 5,4% (див. Рис. 3.2).
Підстава кожного стовпчика малюнка побудовано на інтервалі швидкостей, про який йде мова, а площа пропорційна частці молекул, швидкості яких лежать в цьому інтервалі.
Можна розрахувати і розподіл молекул по різним значенням енергії поступального руху-
Число молекул енергія яких більш ніж в два рази перевершує середню, вже менше 10%. Частка ще більш "енергійних" молекул тане в міру збільшення енергії у все зростаючій мірі. Так, молекул, енергія яких в 4 рази більше середньої, - всього 0,7%, в 8 разів більше середньої - 0,06 * 10-4%, в 16 разів більше середньої - 2 * 10-8%.
Енергія молекули кисню, що рухається зі швидкістю 11 км / с, дорівнює 23 * 10-12 ерг. Середня енергія молекули при кімнатній температурі дорівнює всього 6 * 10-14 ерг. Таким чином, енергія "одинадцяти-кілометрозой молекули" принаймні в 500 разів більше енергії молекули з середньою швидкістю. Не дивно, що частка молекул зі швидкостями вище 11 км / с дорівнює неймовірно малому числу - близько 10-300.
Але чому нас зацікавила швидкість 11 км / с? У книзі 1 ми говорили про те, що відірватися від Землі можуть лише тіла, які мають цю швидкість. Значить, забравшись на велику висоту, молекули можуть втратити зв'язок із Землею і відправитися в далеке міжпланетну подорож, але для цього треба мати швидкість 11 км / с. Частка таких швидких молекул, як ми бачимо, настільки незначна, що небезпека втрати атмосфери Землі не загрожує навіть через мільярди років.
Швидкість догляду атмосфери надзвичайно сильно залежить від гравітаційної енергії γ Mm / r. Якщо середня кінетична енергія молекули в багато разів менше гравітаційної енергії, то відрив молекул практично неможливий. На поверхні Місяця гравітаційна енергія в 20 разів менше, що дає для енергії "тікання" молекули кисню значення 1,15 * 10-12 ерг. Це значення перевищує величину середньої кінетичної енергії молекули всього лише в 20-25 разів. Частка молекул, здатних відірватися від Місяця, дорівнює 10-17. Це вже зовсім не те, що 10-300, і підрахунок показує, що повітря буде досить швидко йти з Місяця в міжпланетний простір. Не дивно, що на Місяці немає атмосфери.
Парканом, з якою теплової швидкістю рухається маленька?

